服務熱線
177-5061-9273

龍腦;冰片;2-莰醇;borneol
分子式 C10H18O
又名冰片、2-莰醇。無色或白色半透明六方形結晶體。有d、l、dl三種旋光異構體。分子量154.25。密度1.011g/cm3。熔點208℃。沸點212-214℃。閃點150℃。不溶于水。溶于乙醇、氯仿、乙醚。具有類似樟腦的氣味。
生產方法:主要采用還原法。以樟腦為原料,先溶于乙醇中,再在金屬鈉存在下,進行還原反應而得。
用途:醇類合成香料。主要用作薰衣草、柑桔古龍香型等香精的調合香料,較多用于爽身粉及牙膏中。也可用作合成樟腦的原料。
龍腦就是冰片,又名片腦、桔片、艾片、龍腦香、梅花冰片、羯布羅香、梅花腦、冰片腦、梅冰等,是由菊科艾納香莖葉或樟科植物龍腦樟枝葉經水蒸汽蒸餾并重結晶而得。亦有用松節油經一系列化學方法工藝而得。其可用于閉證神昏、用于目赤腫痛,喉痹口瘡、用于瘡瘍腫痛,潰后不斂等。天然冰片(右旋龍腦)就是利用其鮮枝葉為原料,采用先進的提取工藝精制而成的純天然制品。歷史上,我國從婆羅洲及蘇門答臘等地獲得天然冰片,故以“龍腦”示其名貴。

龍腦樟樹(Cinnamomum camphora)既是名貴稀有的藥材,又是高級香料,還是重要的化工原料,有植物黃金的美譽。原產于印尼蘇門答臘島的天然龍腦香樹樹根曾經是龍腦的主要來源,但是由于長期過度采伐已近枯竭。龍腦最早記載于南北朝,距今已有兩千多年歷史,在中醫典籍中龍腦被稱為天然冰片,因極具透皮功能,被歸于芳香開竅類藥材。《本草經疏》云:龍腦“其香為百藥之冠。”,我國一直未找到原生記錄,長期依賴于高價進口,近代更被合成冰片所替代。1988年,在湖南新晃侗族自治縣步頭降苗族鄉原始森林中發現的中國第一株富含龍腦的野生樟科植物-----龍腦樟。

龍腦香,又稱為腦子、瑞腦、瑞龍腦等,是龍腦香科植物龍腦香樹Dryobalanops aromatic Gwaertn.f.的樹脂中析出的天然結晶性化合物,也是一種名貴的香藥,古人稱之為:“龍腦”以示其珍貴。上等龍腦香,“狀似云母、色如冰雪”,質地純凈,稱之為“冰片”。
龍腦香的流傳
龍腦香,原產于南洋群島各地,后隨貿易往來進入中原。早在魏晉時期,中國人就認識到龍腦香祛病療疾的功效,自《名醫別錄》首次出現后,就一直沒有缺席本草書籍。除了藥用,龍腦香還頻繁用于隨身佩戴、屋室熏燃、飲食配料等諸多方面,與沉香、檀香、麝香并稱中國四大名香,構成了中國歷史悠久又色彩斑斕的香文化。隨著貿易往來進入中原地區,隋唐時期,龍腦香頻繁被作為“國禮”送給中國皇帝,《隋書·卷八十二列傳第四十七》記載:常駿等人奉隋煬帝之命出使赤土國(指馬來西亞、印度尼西亞),赤土國王派兒子那邪迦“隨并獻金芙蓉冠、龍腦香”。
龍腦香的功用
魏晉時期開始,中國人就與龍腦香結下了不解之緣,龍腦香早已深深植于中國的傳統文化之中,滲透在古人祛病療疾、祝禱祈福、養神養生、日常飲食、人際交往等諸多方面,成為其不可割舍的部分。
(一)祛病
最早見于魏晉陶弘景《名醫別錄》記載:“味辛、苦,微寒,一云溫、平、無毒。”主治心腹邪氣,風濕積聚,耳膚翳。作為醫籍系統介紹了龍腦香性味、主治、產地等信息,也可看出魏晉時期人們就熟悉掌握了龍腦香的藥性主治等,將龍腦香作為藥物使用。明?李時珍《本草綱目》對龍腦香功用主治進行了總結與歸納,龍腦香可內服可外用,內服有開竅醒神、清熱解毒之效。現代藥理研究證明,龍腦香有鎮痛、鎮靜、抗炎、抗菌、抗生育(妊娠中期和晚期有顯著引產作用)的作用。
(二)佩香
中國古代很早就有的風俗,外來香料進入中原以前,人們多將蘭、芷、蕭、柏、艾、郁、椒、桂、辛夷、茅等香草或香木做成香囊佩戴。隋唐時期,隨著龍腦香大量進入中國,佩戴龍腦香成為當時風尚。唐朝皇帝將其賞給后宮、重臣,《酉陽雜俎》記載的玄宗思貴妃的故事正是以龍腦香為線索。
(三)熏燃
宗教有焚香傳統,人們相信,在氤氳香氣中禱告冥想更為靈驗。無論佛教,還是道教,儀式上均可見龍腦香的身影。佛教里,龍腦既是禮佛的上等供品,也是“浴佛”的主要香料之一,還被列入密宗的“五香”(沉香、檀香、丁香、郁金香、龍腦香)。在盛產龍腦的地區,龍腦樹的樹膏也被用作佛燈的燈油。《新五代史》記載了道教做法時焚龍腦數斤:“守元教昶起三清臺三層,以黃金數千斤鑄寶皇及元始天尊、太上老君像,日焚龍腦、薰陸(乳香)諸香數斤,作樂于臺下,晝夜聲不輟,云如此可求大還丹。”
龍腦香的今天
近代以后,香文化斷層,作為香料的龍腦香逐漸淡出人民的視野,但作為藥用卻是剛需,因為中藥的內服外用處方中,出現“冰片”的概率太高了,試舉幾個耳熟能詳的中藥復方或中成藥:復方丹參片(滴丸)、速效救心丸、麝香保心丸、安營牛黃丸、牛黃解毒片、冰硼散、七厘散、生肌散、冠心蘇合丸、蘇合香丸、行軍散、雙料喉風散…… 這些藥中,有上千上萬元一粒者,也有3-5元一瓶的,足見冰片的使用之廣。
為什么會這樣?筆者覺得它的小分子高度親脂性這個特性起到了重要的作用:其一、它是古代較易得的一種有抗菌作用的透皮劑,可打開皮膚角質層,幫助其它藥物進行皮層以內,因此很多外用藥散離不開它,其二,同樣由于它的高度親脂性,它是一種有效的可以透過血腦屏障的藥物,而且可協助其它藥物透過血腦屏障,故而不少心腦血管藥物也少不了它(也許,龍腦香的腦字就這么來的)。
冰片的種類及發展
現在的冰片,有很復雜的來源,成了一個不小的家族:
合成冰片:以松節油、樟腦為原料,經化學合成的方法,得到的薄片狀結晶。
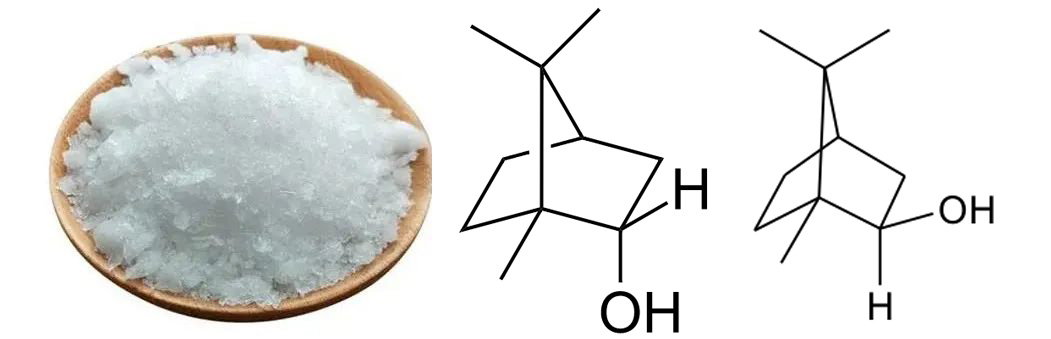
合成冰片,冰片,異冰片
艾片:從廣西、云南等地發現一種菊科植物艾納香,將它的葉子經蒸餾和反復升華,得到的結晶即是艾片。

龍腦樟冰片:從湖南、江西等地發現的數量極其稀少的樟樹,其枝葉經提取、加工后可得天然冰片,以上三種來源的冰片均被收入《中國藥典》一部。


龍腦香冰片:不同于龍腦樟樹,它是龍腦香樹分泌或提取出來的,尷尬的是,龍腦香來源的天然冰片,自2005年以后,在《中國藥典》上找不到它的位置了,龍腦香來的冰片入藥,在中國已無標準可依了,換句話說,它在中國,只能用作香料而不具備官方法定的藥品身份。
也就是說,發展到今天,冰片有四種來源,即龍腦香樹來源、艾納香來源、合成來源、龍腦樟來源。雖然都叫冰片,外表、氣味和標稱的功效都基本相同,但其實它們的內在化學成分是有很大差別的。(表1),從表1可見,傳統的天然龍腦香冰片,是以右旋龍腦為主的;而合成片,主要含的是消旋龍腦(約60)和消旋異龍腦,折合下來,含右旋龍腦不過30%左右,其實它應該不好意思叫冰片;而艾片主要成分是左旋龍腦,基本不含右旋龍腦;倒是精制后的龍腦樟,也是主要含有右旋龍腦(96%以上),可能是最接近傳統的天然龍腦香冰片的來源了。
表1 四種不同來源冰片的比較
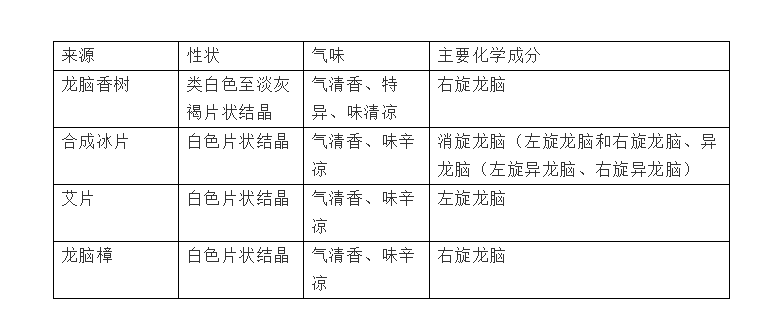
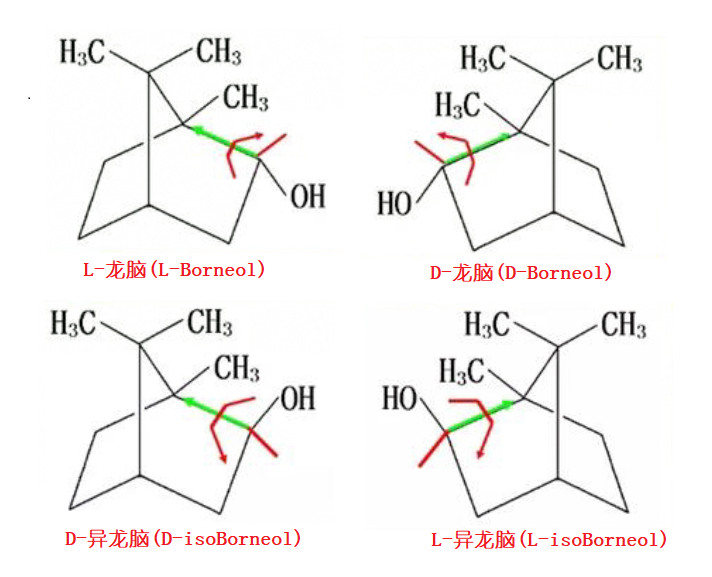
圖1 冰片中含有的D-,L-龍腦以及D-,L-異龍腦成分的結構
使用禁忌
陰虛陽亢、小兒慢涼、脾虛肚瀉、肝腎虛虧者、目疾者忌服冰片,孕婦慎服冰片
冰片的醫用進展概述
冰片又稱龍腦和梅片,外觀呈無色半透明或白色六方形薄片狀,質地松脆,氣味芳香,有強烈清涼感。其化學名為2-莰醇,分子式C10H18O,有右旋、左旋、消旋三種旋光異構體。

按其來源分為左旋龍腦(艾片)、右旋龍腦(天然冰片)和合成龍腦。冰片在我國有著悠久的使用歷史,《新修本草》記載其功效:“主心腹邪氣,風濕積聚,耳聾,明目,去目赤膚翳”;《本草綱目》記載其:“通諸竅,散郁火”,一直以來,冰片素有“引藥上行”和“佐使有功”的功能,因此其常作為佐使藥被廣泛應用。由于冰片具有促進不溶性藥物透皮吸收以及可提高其他藥物的血藥濃度和生物利用度等作用,其在食品和醫藥工業應用非常廣泛,是雙料喉風散、復方丹參滴丸、速效救心丸、麝香保心丸、復方丹參片、心血寧片等60多種名優中成藥的主要成分,起著“藥引”的作用,以增加其他藥物的治療效果。
同名為冰片,差異各不同
左旋龍腦(艾片)為菊科植物艾納香的新鮮葉經提取加工制成的結晶。右旋龍腦(天然冰片)為樟科植物龍腦樟的新鮮枝、葉經提取加工制成。合成龍腦又稱異冰片,則是利用松節油中的α-蒎烯與脫水草酸為原料經過化學方法合成而得,其含左旋龍腦、右旋龍腦以及樟腦成分,因此,合成龍腦是消旋體。這三種冰片是旋光異構體,由于其結構中甲基以及羥基官能團位置的差異導致各自的生物學活性有所區別,同時,由于其來源不同,所含雜質、副產物也有所差別。
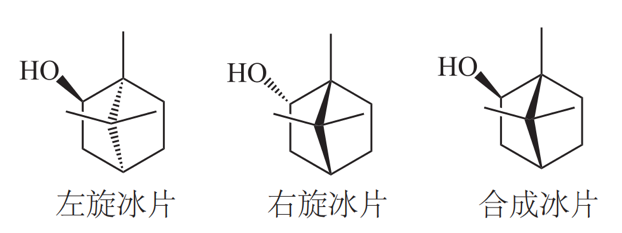
質量差異:根據藥典,天然冰片應含右旋龍腦96%以上,不得檢出異龍腦(異莰醇),可含有3%以下的樟腦;艾片應含左旋龍腦85%以上,可含5%以下的異龍腦和10%以下的樟腦;而合成冰片中消旋龍腦含量僅為55%以上,要求樟腦含量在0.5%以下,為限定異龍腦的含量,往往實際含44%以上的異龍腦。
活性差異:以蛙皮為體外模型,考察了天然冰片和合成冰片對梔子提取物黏膜通透性的影響。結果發現,雖然天然冰片和合成冰片均能夠促進梔子提取物的滲透,但是天然冰片對其具有更好的保護效果,同時隨著天然冰片比例的增加,梔子提取物的黏膜通透性增強,其對梔子苷穩定性的保護作用也增強,而合成冰片無此功效。天然冰片(右旋)和艾片(左旋)間也存在純度和手性的差別。左旋體的藥物在進入人體后的效用往往明顯優于右旋體,而在體外實驗中,艾片針對金黃色葡萄球菌、溶血性鏈球菌、肺炎球菌、白喉桿菌、綠膿桿菌等的抑菌效價也都高于天然冰片。藥典中天然冰片和艾片的功能與主治完全相同,而前者常用量為0.3-0.9g,后者為0.15-0.3g,可以看出左旋冰片前景廣闊,有相當的發展空間。
冰片在抗菌、抗炎、鎮痛方面的應用
冰片對多種常見病菌(如大腸埃希菌、乙型溶血性鏈球菌、金黃色葡萄球菌、真菌等)具有高濃度可殺菌、低濃度可抑菌的功效。冰片抗炎效果顯著,研究顯示口服天然冰片能明顯抑制巴豆油引起的小鼠耳腫脹及醋酸引起的小鼠腹腔毛細血管通透性增加。在腦缺血再灌注的大鼠模型中研究發現,冰片是通過降低包括細胞間黏附分子-1、腫瘤壞死因子-α、白細胞介素-1β、誘導型一氧化氮合酶、環氧化酶-2等炎癥相關細胞因子的表達而實現抗炎的過程。使用大鼠后肢穿透傷疼痛模型,發現冰片外用于損傷部位可顯著提高大鼠的繼發機械痛閾、繼發熱痛閾值,表示冰片可抑制損傷處傷害性感受器的信號轉入,對外傷性急性疼痛起抑制作用。建立小鼠疼痛模型、敲除小鼠TR-PM8基因和藥理學阻斷系列實驗,揭示了外用冰片可激活TR-PM8外周神經元,進而激活脊髓背角突觸前代謝型谷氨酸受體,抑制疼痛神經信號傳遞,從而實現鎮痛作用。
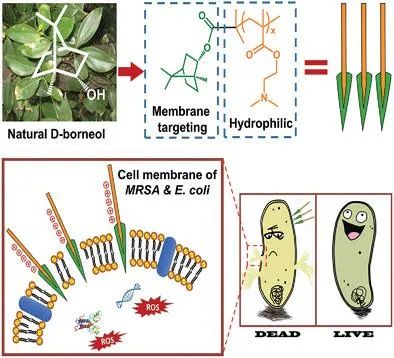
冰片是具有獨特的雙環單萜結構的天然提取物,由于其通過膜破壞機制的廣譜抗菌特性,引起了越來越多的關注。然而,冰片的水溶性可忽略不計限制了其抗菌效率。在此,設計并合成了基于冰片的水溶性抗菌劑,以對抗具有多種耐藥性的細菌。冰片與親水性聚甲基丙烯酸N,N-二甲基乙基酯(PDMAEMA)聚合物鏈的整合增強了冰片對革蘭氏陰性,革蘭氏陽性甚至多藥耐藥細菌的抗菌能力。用冰片基聚合物處理后,耐甲氧西林金黃色葡萄球菌(MRSA)以50 μg mL(-1) 被完全殺死,大腸桿菌以39 μg mL(-1)被消滅。進一步證明,基于冰片的抗菌劑可以作為非浸出抗菌劑接枝到棉織物上,與涂覆有商用季銨整理劑的棉織物(AEM 5700)相比,其具有更高的持續抗菌活性。具有出色殺菌活性(尤其是針對MRSA的殺菌功能)的功能化織物在控制醫院獲得性感染方面可能具有巨大的潛在應用。
冰片在腦部保護作用的應用
冰片對腦缺血小鼠空間分辨學習的影響實驗發現,冰片能有效減少腦缺血再灌注小鼠跳臺實驗中回避反應中的錯誤次數,延長了Y型迷宮實驗中的潛伏期,縮短了逃避時間,表明冰片對缺血再灌注小鼠腦部的神經有著保護作用。研究左旋龍腦、右旋龍腦和合成龍腦3種冰片分別對永久性大腦中動脈閉塞的大鼠神經血管單元中的作用,結果表明左旋龍腦能明顯改善腦缺血后24h的神經功能缺損,左旋龍腦和合成龍腦均能改善腦水腫和腦梗死面積。冰片和腦部保護藥物(如梔子苷和川芎嗪等)在全腦缺血再灌注損傷模型中對神經元的協同保護作用具有區域特異性,在海馬、下丘腦和紋狀體區域的協同作用尤其明顯。
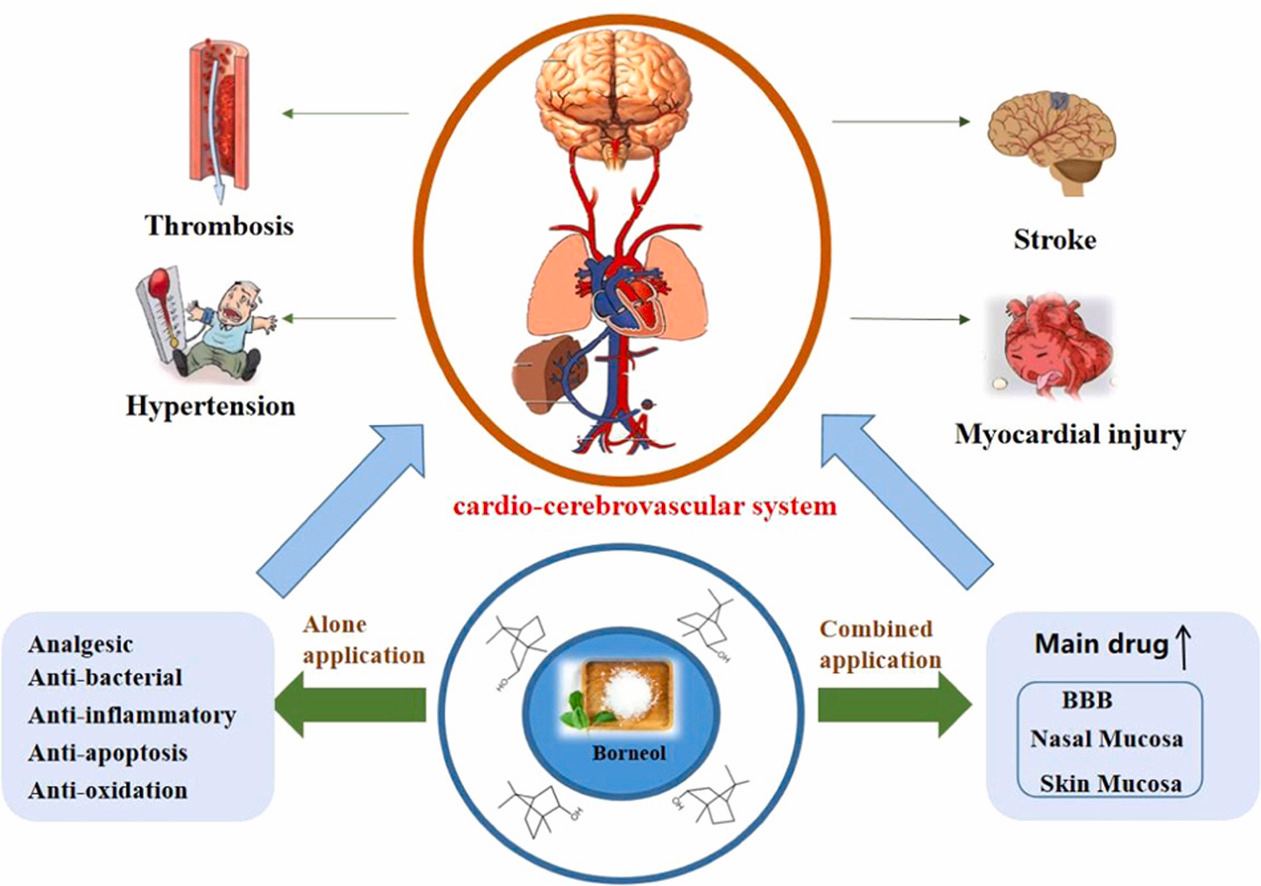
隨著全球人口老齡化進程的加快,心腦血管疾病(CVDs)的發病率呈上升趨勢。它已成為人類死亡的主要原因。冰片(BO)作為一種天然藥物,不僅具有抗炎、抗氧化、抗凋亡、抗凝血等作用,改善能量代謝,還可以促進藥物通過各種生理屏障進入靶器官或組織,如如血腦屏障(BBB)、粘膜、皮膚。因此,它對各種心血管疾病具有顯著的治療作用,這一點已在大量研究中得到證實。然而,BO對心血管疾病的藥理作用和機制尚未得到充分研究。因此,本綜述總結了 BO 的藥理作用和可能的機制。
冰片作為藥物吸收促進劑的應用
冰片在中藥配伍中常用作佐藥幫助其他藥物更好地發揮療效,有著“獨行則勢弱,佐使則有功”的說法。冰片作為芳香開竅中藥代表,有脂溶性強、相對分子質量小、容易揮發、可改變脂質分子的排列和增加其流動性等特點,因而在藥物的透皮吸收方面應用廣泛。冰片可以促進5-氟尿嘧啶、安替比林、阿司匹林、水楊酸和布洛芬等5種模型藥物的體外經皮滲透吸收,其分子機制可能與冰片通過干擾角質層脂鏈的結構,引起皮膚滲透屏障的改變相關。血腦屏障在阻止有害物質由血液進入腦組織的同時也阻止治療性藥物通過血腦屏障,從而可削弱藥物的治療效果。冰片具有雙向調節血腦屏障通透性的作用,既能增加生理性血腦屏障通透性,促使其他藥物通過其而引藥上行,同時也可降低已損傷腦組織的血腦屏障通透性,起到保護腦缺血再灌注后其結構的作用。
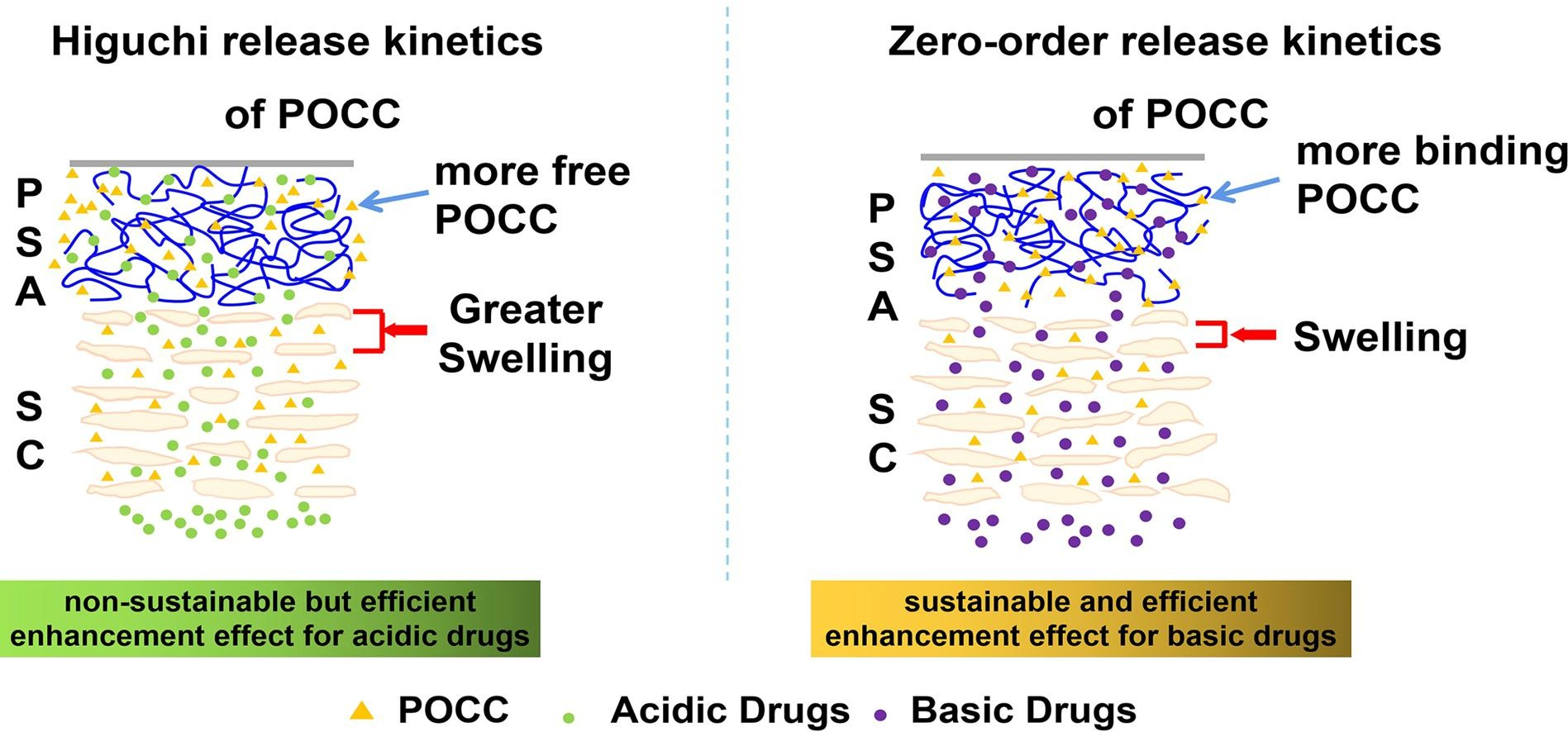
目前,滲透促進劑的釋放動力學如何影響其對藥物皮膚吸收的促進作用及其分子機制尚不清楚。在本文中,滲透促進劑的釋放動力學(的Plurol Oleique CC(POCC)),其涉及的釋放百分比(PR),釋放的持續時間(RD)和釋放動力學常數(?)和對藥物皮膚吸收其增強療效用研究體外皮膚分別進行保留研究和體外皮膚滲透研究。POCC 從酸性藥物加載貼劑中釋放出來,隨后是 Higuchi 釋放模型,并且具有短的RD(8-16 小時),導致其對酸性藥物的增強效率不可持續。然而,從基本藥物加載貼劑中釋放的 POCC 遵循具有長RD(12-24 小時)的零級模型,從而對基本藥物產生可持續且有效的增強效率。創新參數滲透增強系數(C PE)的較低方差代表相對可持續和有效的增強效果,如下所示:0.20(扎托洛芬(ZPF)),0.31(雙氯芬酸(DCF)),0.27(吲哚美辛(IMC) )、0.07 (阿扎司瓊 (AST))、0.11 (奧昔布寧 (OBN)) 和 0.06 (多奈哌齊 (DNP))。根據 FT-IR、MTDSC、13C NMR光譜、分子動力學模擬、SAXS和拉曼成像,Higuchi釋放模型是由酸性藥物和壓敏粘合劑(PSA)之間的強相互作用引起的。這種強相互作用導致 POCC 從酸性藥物加載貼片中擴散速度更快,并使角質層 (SC) 脂質的長周期相 (LPP) 膨脹程度提前達到平臺。零級釋放模型是因為堿性藥物與PSA之間的弱相互作用使得大部分POCC仍然與PSA結合,這反過來導致LPP以緩慢但可持續的過程膨脹。綜上所述,POCC 的零級釋放動力學導致對堿性藥物的持續有效的滲透增強效率,而 Higuchi 釋放動力學對酸性藥物顯示出相反的效果。
冰片作為化療增敏劑的應用
冰片作為一種吸收促進劑,可通過抑制多藥耐藥蛋白的過度表達,單獨或與其他佐劑合用,增強腫瘤細胞對化療藥物的敏感性。冰片聯合長春新堿能夠顯著提高長春新堿的抗腫瘤活性,冰片在增敏過程中的作用機制可能與其顯著抑制P-gp活性有關。冰片聯合順鉑能夠顯著增加順鉑抑制大鼠C6腦膠質瘤生長能力,其作用機制可能與冰片通過促進順鉑透過血腦屏障后累積,從而在膠質瘤部位發揮作用有關。

盡管有效靶向了表皮生長因子受體(EGFR),但由于在腫瘤區域的藥物蓄積不足,因此將吉非替尼(GFT)用于非小細胞肺癌(NSCLC)治療仍然失敗。因此,迫切需要開發具有協同治療作用的GFT化學增敏劑,以用于晚期癌癥治療。在本文中,將天然化學增敏劑天然冰片(NB)配制成水包油納米乳液,以增強其溶解度,分布并最終提高GFT的治療指數。通過蛋白質組學研究揭示,通過選擇性鑒定A549 NSCLC細胞中的八個特定蛋白質靶標,NB(NBNPs)的納米化顯示出比NB更強的靶向遞送和細胞毒性。NBNP通過有效調節EGFR / EHD1介導的A549 NSCLC細胞凋亡,實現了比GFT NB更強的化學增敏作用。由于NBNP和GFT之間令人滿意的協同作用,因此聯合療法不僅增強了GFT對NSCLC增殖的抗癌能力,而且避免了體內的嚴重雙重毒性。這一發現證明了NBNPs與GFT之間的有效協同作用,并進行了明確的機理研究,并有望擴展NBNPs作為晚期癌癥化療的新型化學增敏劑的應用。該聯合療法不僅增強了GFT對NSCLC增殖的抗癌能力,而且避免了體內嚴重的雙重毒性。這一發現證明了NBNPs與GFT之間的有效協同作用,并進行了明確的機理研究,并有望擴展NBNPs作為晚期癌癥化療的新型化學增敏劑的應用。該聯合療法不僅增強了GFT對NSCLC增殖的抗癌能力,而且避免了體內嚴重的雙重毒性。這一發現證明了NBNPs和GFT之間有效的協同作用,并進行了明確的機理研究,并有望擴展NBNPs作為晚期癌癥化療的新型化學增敏劑的應用。
冰片促進納米藥物吸收與傳遞
冰片具有促進不溶性藥物透皮吸收以及可提高其他藥物的血藥濃度和生物利用度等作用。經過冰片修飾或將冰片做成復合納米體系后,納米藥物的細胞和組織穿透能力得到增強,藥效學活性也有所提高。因此,基于冰片強大的促透能力,在納米藥物中引入冰片,這將有望提高納米藥物的跨膜吸收及向腫瘤組織的遞送量。有研究在神經毒素納米體系中通過物理方法混合了冰片-薄荷腦共熔物,證實了此吸收促進劑能明顯地促進藥物跨過血腦屏障,提高藥物在腦部的積累含量。通過對比冰片修飾和非冰片修飾的昔洛韋固體脂質納米粒在小鼠腦部的分布情況發現,冰片通過微乳液法混合修飾的納米系統更能增加昔洛韋向腦部的遞送。
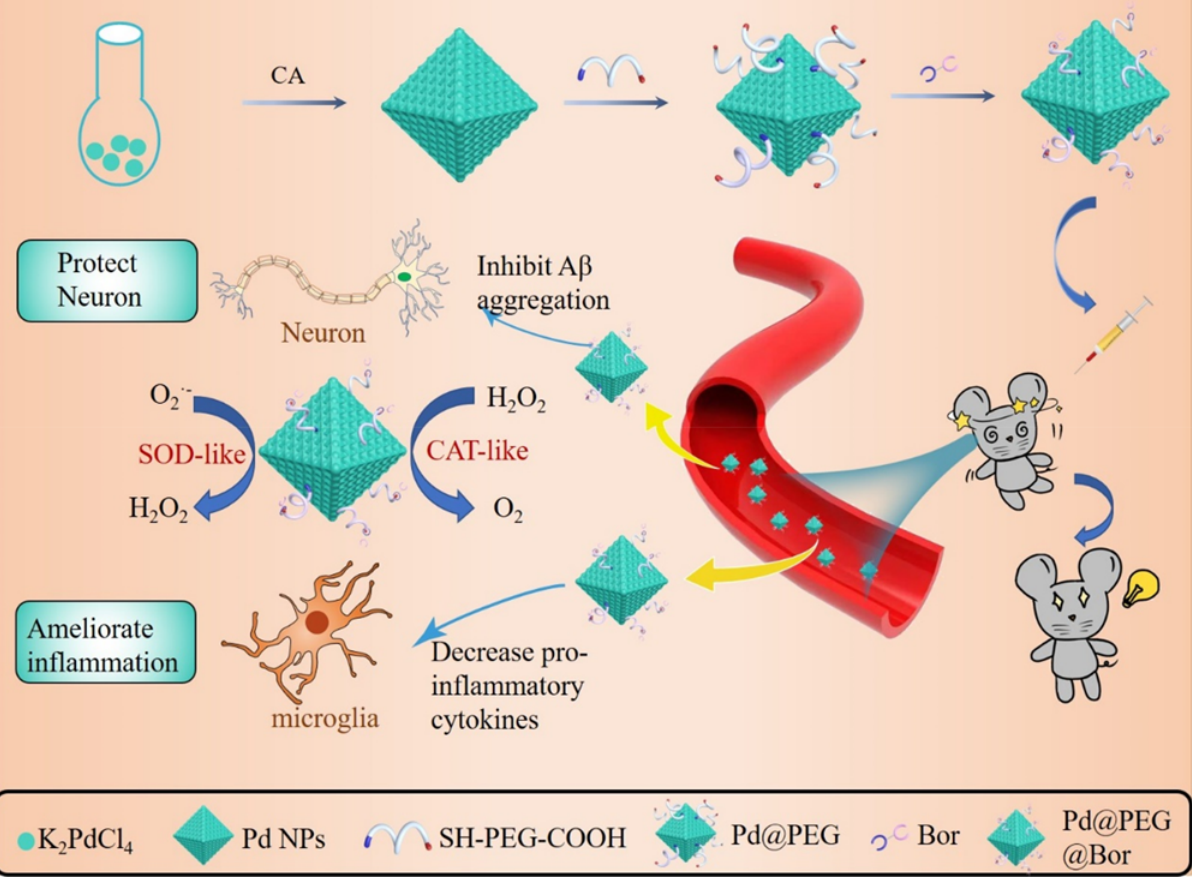
2021年10月,來自暨南大學的研究團隊在《ACS APPLIED MATERIALS&INTERFACES》發表了論文“A Functionalized Octahedral Palladium Nanozyme as a Radical Scavenger forAmeliorating Alzheimer’s Disease”。在這項研究中,研究者們設計并制備了八面體鈀(Pd)納米酶復合材料(Pd@PEG@ Bor),將中藥成分冰片(Bor)偶聯在Pd@PEG納米材料的表面用于提高穿過血腦屏障和靶向神經元的效率。
研究者們分別從抗氧化、生物相容性、消除ROS、血腦屏障透過實驗、小鼠行為學等方面表征了復合材料的生物學性能,證明了這種復合材料能提高穿過血腦屏障的效率以及靶向神經元,消除細胞內過多的ROS,維持線粒體膜電位和鈣離子水平,抑制Aβ的產生和聚集,減少神經炎癥,保護神經元,并進一步改善AD小鼠的認知障礙,可以有效緩解AD的癥狀。
冰片是我國傳統中藥,具有提神醒腦、芳香開竅等作用,對小腦血管疾病以及外用治療燒燙傷都具有顯著的積極作用。現代藥理學研究表明,冰片不僅具有抗菌、抗炎、鎮痛等直接治療作用,還能夠促進藥物透皮吸收,雙向調節血腦屏障通透性,增強藥物活性,從而提高藥物的治療效果。隨著研究的深入,冰片在癌癥化療增敏劑方面也表現出巨大的潛在應用價值。通過對冰片進行納米化劑型改造,或用冰片修飾納米轉運系統增強藥物作用效果,這為冰片作為化療增敏劑的開發及其他藥物領域應用方面提供了新策略。
參考文獻:
Liu Yang,Chengdong Zhan,Xiangyue Huang,Liangzhi Hong,Liming Fang,Wen Wang,Jianyu Su. Durable Antibacterial Cotton Fabrics Based on Natural Borneol-Derived Anti-MRSA Agents. Advanced Healthcare Materials. 2020, 9, 11, 2000186.
Songyu Liu, Yu Long, Shuang Yu, Dingkun Zhang, Qiyue Yang, Zhimin Ci, Mingquan Cui, Yulu Zhang, Jinyan Wan, Dan Li, Ai Shi, Nan Li, Ming Yang, Junzhi Lin. Borneol in cardio-cerebrovascular diseases: Pharmacological actions, mechanisms, and therapeutics. Pharmacological Research. 2021, 169, 105627.
Jiuheng Ruan, Chao Liu, Haoyuan Song, Ting Zhong, Peng Quan, Liang Fang.Sustainable and efficient skin absorption behaviour of transdermal drug: The effect of the release kinetics of permeation enhancer. International Journal of Pharmaceutics . 2022, 612, 121377.
Riming Yuan,Yanyu Huang,Leung Chan,Dihao He,Tianfeng Chen.
Engineering EHD1-Targeted Natural Borneol Nanoemulsion Potentiates Therapeutic Efficacy of Gefitinib against Nonsmall Lung Cancer. ACS Appl. Mater. Interfaces . 2020, 12, 41, 45714–45727.
Zhi Jia, Xiaoyu Yuan, Ji-an Wei, Xian Guo, Youcong Gong, Jin Li, Hui Zhou, Li Zhang*, and Jie Liu*. A Functionalized Octahedral Palladium Nanozyme as a Radical Scavenger for Ameliorating Alzheimer’s Disease. ACS Appl. Mater. Interfaces . 2021, 13, 42, 49602–49613